2026 Autor: Howard Calhoun | calhoun@techconfronts.com. E modifikuara e fundit: 2025-01-24 13:25:33
Disociimi elektrik luan një rol të madh në jetën tonë, megjithëse zakonisht nuk mendojmë për të. Është me këtë fenomen që lidhet përçueshmëria elektrike e kripërave, acideve dhe bazave në një mjedis të lëngshëm. Nga rrahjet e para të zemrës të shkaktuara nga elektriciteti "i gjallë" në trupin e njeriut, i cili është tetëdhjetë për qind i lëngshëm, te makinat, celularët dhe lojtarët, bateritë e të cilave në thelb janë bateri elektrokimike, disociimi elektrik është i padukshëm kudo pranë nesh.
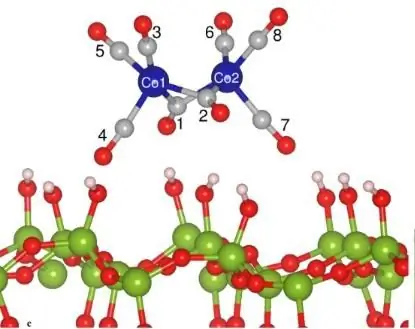
Në enë gjigante që lëshojnë tym toksik nga boksiti i shkrirë në temperatura të larta, metali "me krahë" - alumini përftohet me elektrolizë. Gjithçka rreth nesh, nga grilat e kromit të radiatorit deri te vathët e argjendtë në veshët tanë, një herëose ballafaquar me solucione ose kripëra të shkrira, dhe kështu me këtë fenomen. Jo më kot disociimi elektrik studiohet nga një degë e tërë e shkencës - elektrokimia.
Kur treten, molekulat e lëngut tretës hyjnë në një lidhje kimike me molekulat e substancës së tretur, duke formuar solvate. Në një tretësirë ujore, kripërat, acidet dhe bazat janë më të ndjeshme ndaj shpërbërjes. Si rezultat i këtij procesi, molekulat e lëndës së tretur mund të dekompozohen në jone. Për shembull, nën ndikimin e një tretësi ujor, jonet Na+ dhe CI- në kristalin jonik NaCl kalojnë në mjedisin tretës në një cilësi e re e grimcave të tretshme (të hidratuara).
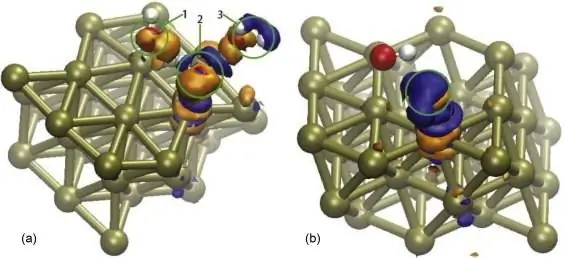
Ky fenomen, i cili në thelb është procesi i zbërthimit të plotë ose të pjesshëm të një lënde të tretur në jone si rezultat i veprimit të një tretësi, quhet "shpërbërje elektrike". Ky proces është jashtëzakonisht i rëndësishëm për elektrokiminë. Me rëndësi të madhe është fakti që shpërbërja e sistemeve komplekse shumëkomponente karakterizohet nga një rrjedhje hap pas hapi. Me këtë fenomen vërehet edhe një rritje e mprehtë e numrit të joneve në tretësirë, gjë që i dallon substancat elektrolitike nga ato joelektrolitike.
Në procesin e elektrolizës, jonet kanë një drejtim të qartë të lëvizjes: grimcat me ngarkesë pozitive (kationet) - në një elektrodë të ngarkuar negativisht, të quajtur katodë, dhe jonet pozitive (anionet) - në anodë, një elektrodë me ngarkesë të kundërt, ku ato shkarkohen. Kationet reduktohen dhe anionet oksidohen. Prandaj, disociimi është një proces i kthyeshëm.
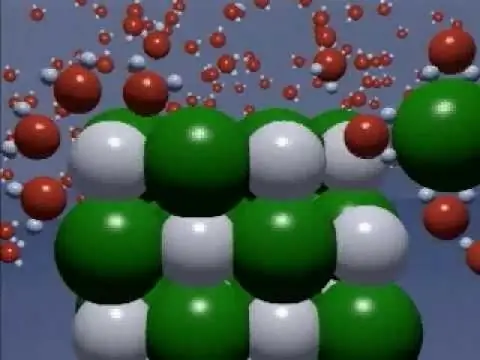
Një nga karakteristikat themelore të këtij procesi elektrokimik është shkalla e shpërbërjes elektrolitike, e cila shprehet si raport i numrit të grimcave të hidratuara me numrin total të molekulave të substancës së tretur. Sa më i lartë ky tregues, aq më i fortë është elektroliti kjo substancë. Mbi këtë bazë, të gjitha substancat ndahen në elektrolite të dobët, me forcë mesatare dhe të fortë.
Shkalla e shpërbërjes varet nga faktorët e mëposhtëm: a) natyra e substancës së tretur; b) natyrën e tretësit, konstantën dielektrike dhe polaritetin e tij; c) përqendrimi i tretësirës (sa më i ulët ky tregues, aq më e madhe është shkalla e disociimit); d) temperaturën e mjedisit tretës. Për shembull, shpërbërja e acidit acetik mund të shprehet me formulën e mëposhtme:
CH3COOH H+ + CH3COO-
Elektrolitet e forta shpërndahen pothuajse në mënyrë të pakthyeshme, pasi tretësira e tyre ujore nuk përmban molekulat origjinale dhe jonet e pahidratuara. Duhet shtuar gjithashtu se të gjitha substancat që kanë një lloj lidhjesh kimike jonike dhe kovalente polare i nënshtrohen procesit të disociimit. Teoria e disociimit elektrolitik u formulua nga fizikani dhe kimisti i shquar suedez Svante Arrhenius në 1887.
Recommended:
Procesi i planifikimit strategjik përfshin Hapat dhe bazat e planifikimit strategjik

Në shumë mënyra, suksesi i kompanisë në treg përcakton planifikimin strategjik në organizatë. Si metodë, është një studim dhe teknikë hap pas hapi e ekzekutimit të një procedure që synon ndërtimin teorik dhe praktik të një modeli të së ardhmes së kompanisë. Një program i qartë për kalimin e një organizate apo ndërmarrjeje në një model menaxhimi optimal në treg
Etika e kreut: bazat e komunikimit të biznesit, motivimi i stafit dhe marrëdhëniet e shërbimit

Për të kuptuar se çfarë është etika e menaxhimit të një drejtuesi, duhet të jeni në gjendje të artikuloni qartë se cili është thelbi i punës së një personi të tillë. Udhëheqja është një koncept që përfshin aktivitetet organizative dhe koordinimin e aktiviteteve të personelit të punësuar nga një person ose një grup njerëzish të specializuar në zgjidhjen e çështjeve menaxheriale
Bazat e biznesit dhe sipërmarrjes

Sot, elementi përcaktues i aktivitetit ekonomik është të bërit biznes. Ky artikull diskuton aspektet përcaktuese të menaxhimit të strukturave ekonomike, tiparet e formimit dhe zhvillimit të suksesshëm të një personi juridik, si dhe faktorët nga të cilët varet produktiviteti i një ndërmarrje
Analiza e veprimtarive financiare dhe ekonomike - bazat teorike

Tranzicioni në marrëdhëniet e tregut kërkon që të gjitha ndërmarrjet të rrisin efikasitetin e prodhimit, gjë që, nga ana tjetër, do të rrisë konkurrencën e produkteve të tyre. Rolin më të rëndësishëm në zgjidhjen e këtij problemi e luan analiza e aktivitetit financiar dhe ekonomik. Me ndihmën e kësaj disipline shkencore zhvillohen planet strategjike të zhvillimit, arsyetohen shkencërisht vendimet e menaxhimit dhe monitorohet zbatimi i tyre
Çfarë është një ngritës elektrik? Ngritës elektrik për ngritjen vertikale të ngarkesave

Artikulli i kushtohet ngritjes elektrike. Dizajni i njësisë ngritëse, aftësitë e tij operacionale dhe varietetet merren parasysh

